Amgen Worldwide
A biotechnology pioneer since 1980, Amgen has reached millions of patients around the world.
オンラインリソース
アムジェンは、患者さんが関心のある分野について学べるよう、多数のリソースを用意しております。
A biotechnology pioneer since 1980, Amgen has reached millions of patients around the world.
アムジェンは、患者さんが関心のある分野について学べるよう、多数のリソースを用意しております。
アムジェン株式会社(本社:東京、代表取締役社長:スティーブ・スギノ)と株式会社JMDC(本社:東京都港区、代表取締役社長兼CEO:松島陽介、以下「JMDC」)はこの度、LINE公式アカウント「片頭痛@LINEヘルスケア」(監修:日本頭痛学会、運営:LINEヘルスケア株式会社、コンテンツ提供:アムジェン株式会社、LINEヘルスケア株式会社)の新たなコンテンツとして、「片頭痛リスク予報サービス(Health Weather®)」を開発し提供を開始しました。
「片頭痛リスク予報サービス(Health Weather®)*」は、医療ビッグデータ業界のパイオニアJMDCが保有する「医療ビッグデータ」(累積約1,300 万人分のレセプトデータ)と、一般財団法人日本気象協会(以下、「日本気象協会」)が保有する「気象データ」(分単位で収集される国内外の気象データ)を掛け合わせ、疾患と気象条件の相関関係を統計的に解析することで、片頭痛の発症・重症化リスクを予測するAIモデルを活用したサービスです**。
* Health Weather®:気象と疾患(片頭痛、ぜんそく、アレルギー性疾患等)の関係を分析・予測するJMDCと日本気象協会の共同サービスの総称
** 本サービスは、疾病の診断、治療、予防を目的としていません。
本サービスはLINEヘルスケア株式会社が運営するLINE公式アカウント「片頭痛@LINEヘルスケア」の新たなコンテンツとして追加され、ユーザーの位置情報から週間の片頭痛リスク予報を提供していきます。この度のサービス提供を通じて、アムジェン株式会社、JMDC、日本気象協会、およびLINEヘルスケア株式会社は、「片頭痛@LINEヘルスケア」でユーザーから収集した「頭痛ダイアリー」のデータに基づき、「片頭痛リスク予報」のモデルの更なる精緻化に共同で取り組んでいく予定です※。
片頭痛は神経疾患のひとつで、頭部の片側または両側に反復性の痛み発作を生じます。日本ではおよそ840万人の成人が片頭痛に悩まされていると推計されています1。頭痛の誘因は、ストレスや生活環境、その日の体調など様々ですが、気象の変化も影響があることが知られています。気象の変化による頭痛リスクが事前に把握できることで、頭痛の発症をより良くコントロールできるようになることが期待されます。
アムジェン株式会社では、「To serve patients – 患者さんのために、今できるすべてを」というミッションのもと、今後も治療薬の開発と提供にとどまらない、患者さんの片頭痛コントロールをトータルサポートするための活動に取り組んでまいります。
【片頭痛@LINEヘルスケア】
LINE公式アカウント URL:https://lin.ee/kefKGdP
 |
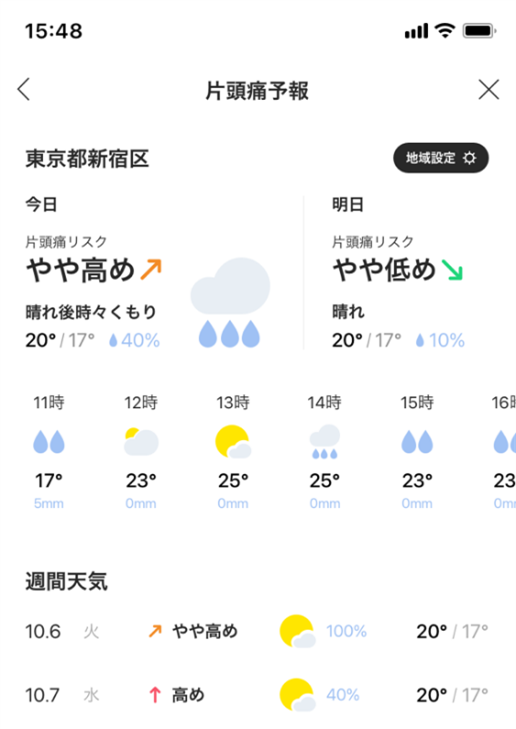 |
片頭痛@LINEヘルスケア「片頭痛リスク予報サービス」(画面イメージ)
片頭痛について
片頭痛は神経疾患であり、中等度から重度の頭部痛の反復性発作を伴います。通常は拍動性で、しばしば片側性であり、悪心、嘔吐、光、音、匂いへの過敏症を伴います2,3。片頭痛は個人的な苦痛、障害、生活の質の低下、社会的・経済的コストと関連しています4。慢性的な片頭痛による経済損失は年間2兆円という試算もあり、個人の日常業務遂行能力を妨げるような深刻な影響を及ぼします5。世界保健機関(WHO)の報告によると、片頭痛は男女ともに障害生存年数の原因疾患トップ2に数えられ、未だ十分な理解と治療が確立されていません4,6。
アムジェン株式会社について
アムジェン株式会社は、世界最大規模の独立バイオテクノロジー企業である米国アムジェン社の日本法人です。2013年10月にアステラス製薬との合弁会社であるアステラス・アムジェン・バイオファーマとして事業を開始し、2020年4月1日にアムジェン社の完全子会社となり商号を変更しました。アムジェン株式会社では、循環器疾患、がん、骨疾患、炎症・免疫性疾患、神経疾患を始めとするアンメット・メディカル・ニーズが高い領域に焦点を絞り、現在600人を超える従業員が、「To serve patients – 患者さんのために、今できるすべてを」というミッションのもと、臨床開発から販売までの活動を行っています。
株式会社JMDCについて
医療ビッグデータ業界のパイオニアとして2002年に設立。独自の匿名化処理技術とデータ分析集計技術を有しています。6 億 5,000 万件以上のレセプトデータと 2,800 万件以上の健診データ(2021 年 3 月時点)に基づく保険者向け保健事業支援、医薬品の安全性評価や医療経済分析などの情報サービスを展開しています。また、健康度の単一指標(健康年齢)や健康増進を目的としたWebサービス(Pep Up)など、医療データと解析力で健康社会の実現に取り組んでいます。
URL:https://www.jmdc.co.jp/
アムジェン社について
アムジェン社は、重篤な疾患に苦しむ患者さんのために、生物学的に革新的な治療を探索・開発・製造・提供する可能性を切り開いていきます。このアプローチは、疾患の複雑性の解明と人体の生物学上の基本を理解するために、先進的なヒト遺伝学などの手法を活用することから始まります。
アムジェン社は、アンメット・メディカル・ニーズが大きい領域に焦点を絞り、生物製剤の製造に関する専門知識を活用して医療効果の向上と人々の生活に画期的な改善をもたらすソリューションを追求しています。1980年に創業したバイオテクノロジーのパイオニアであるアムジェン社は、世界最大の独立バイオテクノロジー企業に成長し、世界中の多くの患者さんに貢献しており、革新的な可能性が期待されるパイプラインを開発しています。
詳細については www.amgen.comをご覧になるか、ツイッターアカウント(www.twitter.com/amgen)をフォローしてください。
※LINE公式アカウント「片頭痛@LINEヘルスケア」のお客様情報取り扱いについて
「片頭痛@LINEヘルスケア」はLINEヘルスケア株式会社が運営しており、「片頭痛@LINEヘルスケア」におけるお客様情報は、片頭痛@LINEヘルスケアプライバシーポリシーに従って適切に取り扱われます。
将来予想に関する記述(アムジェン社)
This news release contains forward-looking statements that are based on the current expectations and beliefs of Amgen. All statements, other than statements of historical fact, are statements that could be deemed forward-looking statements, including any statements on the outcome, benefits and synergies of collaborations, or potential collaborations, with any other company (including BeiGene, Ltd., Kyowa Kirin Co., Ltd., or any collaboration to manufacture therapeutic antibodies against COVID-19), the performance of Otezla® (apremilast) (including anticipated Otezla sales growth and the timing of non-GAAP EPS accretion), the Five Prime Therapeutics, Inc. acquisition, or the Teneobio, Inc. acquisition, as well as estimates of revenues, operating margins, capital expenditures, cash, other financial metrics, expected legal, arbitration, political, regulatory or clinical results or practices, customer and prescriber patterns or practices, reimbursement activities and outcomes, effects of pandemics or other widespread health problems such as the ongoing COVID-19 pandemic on our business, and other such estimates and results. Forward-looking statements involve significant risks and uncertainties, including those discussed below and more fully described in the Securities and Exchange Commission reports filed by Amgen, including our most recent annual report on Form 10-K and any subsequent periodic reports on Form 10-Q and current reports on Form 8-K. Unless otherwise noted, Amgen is providing this information as of the date of this news release and does not undertake any obligation to update any forward-looking statements contained in this document as a result of new information, future events or otherwise.
No forward-looking statement can be guaranteed and actual results may differ materially from those we project. Discovery or identification of new product candidates or development of new indications for existing products cannot be guaranteed and movement from concept to product is uncertain; consequently, there can be no guarantee that any particular product candidate or development of a new indication for an existing product will be successful and become a commercial product. Further, preclinical results do not guarantee safe and effective performance of product candidates in humans. The complexity of the human body cannot be perfectly, or sometimes, even adequately modeled by computer or cell culture systems or animal models. The length of time that it takes for us to complete clinical trials and obtain regulatory approval for product marketing has in the past varied and we expect similar variability in the future. Even when clinical trials are successful, regulatory authorities may question the sufficiency for approval of the trial endpoints we have selected. We develop product candidates internally and through licensing collaborations, partnerships and joint ventures. Product candidates that are derived from relationships may be subject to disputes between the parties or may prove to be not as effective or as safe as we may have believed at the time of entering into such relationship. Also, we or others could identify safety, side effects or manufacturing problems with our products, including our devices, after they are on the market.
Our results may be affected by our ability to successfully market both new and existing products domestically and internationally, clinical and regulatory developments involving current and future products, sales growth of recently launched products, competition from other products including biosimilars, difficulties or delays in manufacturing our products and global economic conditions. In addition, sales of our products are affected by pricing pressure, political and public scrutiny and reimbursement policies imposed by third-party payers, including governments, private insurance plans and managed care providers and may be affected by regulatory, clinical and guideline developments and domestic and international trends toward managed care and healthcare cost containment. Furthermore, our research, testing, pricing, marketing and other operations are subject to extensive regulation by domestic and foreign government regulatory authorities. Our business may be impacted by government investigations, litigation and product liability claims. In addition, our business may be impacted by the adoption of new tax legislation or exposure to additional tax liabilities. If we fail to meet the compliance obligations in the corporate integrity agreement between us and the U.S. government, we could become subject to significant sanctions. Further, while we routinely obtain patents for our products and technology, the protection offered by our patents and patent applications may be challenged, invalidated or circumvented by our competitors, or we may fail to prevail in present and future intellectual property litigation. We perform a substantial amount of our commercial manufacturing activities at a few key facilities, including in Puerto Rico, and also depend on third parties for a portion of our manufacturing activities, and limits on supply may constrain sales of certain of our current products and product candidate development. An outbreak of disease or similar public health threat, such as COVID-19, and the public and governmental effort to mitigate against the spread of such disease, could have a significant adverse effect on the supply of materials for our manufacturing activities, the distribution of our products, the commercialization of our product candidates, and our clinical trial operations, and any such events may have a material adverse effect on our product development, product sales, business and results of operations. We rely on collaborations with third parties for the development of some of our product candidates and for the commercialization and sales of some of our commercial products. In addition, we compete with other companies with respect to many of our marketed products as well as for the discovery and development of new products. Further, some raw materials, medical devices and component parts for our products are supplied by sole third-party suppliers. Certain of our distributors, customers and payers have substantial purchasing leverage in their dealings with us. The discovery of significant problems with a product similar to one of our products that implicate an entire class of products could have a material adverse effect on sales of the affected products and on our business and results of operations. Our efforts to collaborate with or acquire other companies, products or technology, and to integrate the operations of companies or to support the products or technology we have acquired, may not be successful. A breakdown, cyberattack or information security breach could compromise the confidentiality, integrity and availability of our systems and our data. Our stock price is volatile and may be affected by a number of events. Global economic conditions may magnify certain risks that affect our business. Our business performance could affect or limit the ability of our Board of Directors to declare a dividend or our ability to pay a dividend or repurchase our common stock. We may not be able to access the capital and credit markets on terms that are favorable to us, or at all.
The scientific information discussed in this news release related to our product candidates is preliminary and investigative. Such product candidates are not approved by the U.S. Food and Drug Administration, and no conclusions can or should be drawn regarding the safety or effectiveness of the product candidates. Further, any scientific information discussed in this news release relating to new indications for our products is preliminary and investigative and is not part of the labeling approved by the U.S. Food and Drug Administration for the products. The products are not approved for the investigational use(s) discussed in this news release, and no conclusions can or should be drawn regarding the safety or effectiveness of the products for these uses.
注意事項(アムジェン株式会社)
このニュースリリースに含まれている医薬品(開発中のものを含む)に関する情報は、宣伝広告、医学的アドバイスを目的とするものではありません。
###
この件に関するお問い合わせ先
アムジェン株式会社(東京)
コーポレート・アフェアーズ
TEL 03-5293-9516
株式会社JMDC 経営管理部 広報担当
TEL 03-5733-5010
Email jmdc-pr@jmdc.co.jp
REFERENCE